بـــــــرق
تحقیقبـــــــرق
تحقیقاتم بوهر و رادرفورد
تاریخچه
مشاهده و مطالعه پدیده های میکروسکوپیک ، دانشمندان را آگاه ساخت که اتم ، ساختمان درونی مفصلی دارد و موثرترین کار را در این زمینه "ارنست رادرفورد" دانشمند انگلیسی در سال 1911 میلادی و "نیلسن بوهر" دانشمند دانمارکی در سال 1913 میلادی انجام دادهاند.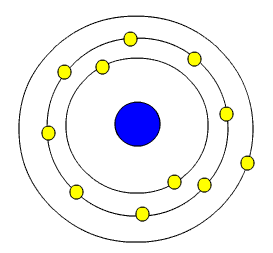
طرح پیشنهادی رادرفورد و بوهر
طرح پیشنهادی ساختمان داخلی اتم)) به توسط دو دانشمند اخیر بصورت زیر بیان می شود:- اتم از یک هسته مرکزی ، مرکب از ذراتی که آنها را نوکلئون مینامیم، تشکیل میشود که در اطراف آن ، تعدادی الکترون دوران میکنند. نوکلئونها که کلیه جرم مادی اتم به آنها مربوط است، بر دو نوعاند: یکی ، پروتون که دارای بار الکتریکی مثبت است و دیگری نوترون که بار الکتریکی ندارد و ذره خنثی میباشد. تعداد الکترونهایی که در اطراف هسته اتم دوران میکنند، مساوی است با تعداد پروتونهای آن.
- الکترونهای هر اتم روی مدارهایی به شکل بیضی دوران میکنند و هسته اتم در یکی از کانونهای بیضی قرار گرفته است.
- الکترونها علاوه بر حرکت انتقالی به دورهسته ، یک حرکت وضعی نیز به دور خود دارند.
- مدارهای الکترونی اتمی هر عنصر ، وضع کاملاً مشخص و ثابتی دارند و آنها را مدار متعادل الکترونی مینامند و الکترونها فقط روی مدارهای متعادل ممکن است بطور ثابت دوران کنند.
- دوران الکترونها روی مدار متعادل ، با انتشار پرتوهای الکترومغناطیسی همراه نیست. (به عبارتی اتم ، تابش ندارد.)
- هر چند مدار متعادل که فاصله آنها از هسته یکسان است، یک لایه الکترونی تشکیل میدهند.
- لایههای الکترونی را از داخل به خارج به ترتیب با حروف Q , P , O , N , M , L, K نمایش میدهند.
- هر گاه شماره ترتیب لایه معینی را با عدد n نمایش دهیم، حداکثر تعداد الکترونها که در هر لایه ممکن است وجود داشته باشد، مساوی است با: 2n2
- حداکثر الکترونهایی که ممکن است در خارجیترین لایه الکترونی اتم وجود داشته باشند، به استثنای لایه k که دو الکترون دارد، هشت میباشد و در صورتی تعداد الکترونهای یک لایه الکترونی ممکن است از 8 تجاوز کند که لایه بعدی آن تشکیل شده باشد .
بررسی مدلهای اتمی
اگر مدل اتمی اخیر در مورد اتم هیدروژن (Hydrogen) بررسی شود، در مییابیم که این اتم دارای یک الکترون است که در لایه k اتمی قرار گرفته است و این لایه اتمی در اتم هلیوم (Helium) بوسیله دو الکترون ، کاملاً پر ( لایه بسته ) میشود.از لیتیوم (Lithium) به بعد ، الکترونهایی که اضافه بر ظرفیت لایه k وجود دارند، در لایه L قرارمیگیرند تا اینکه این لایه نیز در اتم نئون (Neon) با هشت الکترون اشباع میشود که اتم بعدی سدیم (Sodium) با یازده الکترون ، ساختمانی شبیه هیدروژن دارد، زیرا لایههای داخلی آن که نئون را تشکیل میدادند، زیاد روی خواص اتم تاثیر ندارند و تک الکترون لایه آخر ، بیانگر ظرفیت اتم سدیم میباشد.
مولکول
کوچکترین ذره از هر عنصر ساده که ممکن است در واکنشهای شیمیایی وارد شود، به نام اتم و کوچکترین مقداری از جسم خالص که میتواند بطور آزاد وجود داشته باشد، به نام مولکول خوانده میشود.مفاهیم پایه
سیارات ، ماه ، خورشید ، ستارگان ، امواج خروشان دریاها ، کوهها ، صخرههای عظیم ، درههای عمیق ، گلبرگهای فرحانگیز و زیبا ، سنگ ، شیشه ، آجر و حتی هوایی که دائم از آن استفاده میکنیم، از میلیونها میلیون مولکول و اتم تشکیل شده است.قطر یک اتم تقریباً یک ده میلیونم میلیمتر (یک آنگستروم)) و قطر زمین ، 12000 کیلومتر است. به عبارتی یک اتم در برابر سیب همانند یک سیب در برابر کره زمین است. یک گرم آهن از (1022) اتم تشکیل یافته است و حال آنکه این یک گرم آهن مکعب کوچکی است که ابعاد آن از نیم سانتیمتر تجاوز نمی کند. بنابر این در طول یک سانتیمتر آهن میتوان 40 میلیون اتم آهن را پهلو به پهلو جای داد.
همچنین اگر یک گرم آهن را در یک ردیف پهلو هم بگذارند، فاصله ای بدست میآید که 300 سال طول میکشد تا یک هواپیمای جت مافوق صوت آنرا طی کند. هر گاه یک گرم دوده ای که از دودکش یک منزل مسکونی شهر تهران خارج میشود بطور یکنواخت در تمام شهر پخش شود، در هر سانتی متر مربع ، 500 میلیارد اتم کربن وجود خواهد داشت.
ابعاد اتمی
قطر اتم حدوداً یک آنگسترم است. تازه این اتم خودش ساده نیست و قطر هسته آن ، صد هزار مرتبه از قطر خودش کوچکتر است و ما بین هسته و الکترونها ، فضای خالی وسیعی وجود دارد. اگر یک اتم را به قدری بزرگ کنیم که داخل آن دیده شود، مثلاً به اندازه سالن سینما ، خواهیم دید که تمام فضای آن خالی است. فقط در مرکز سالن ، یک ذره کوچک با ابعاد خیلی کوچک که آنرا هسته مرکزی مینامند، وجود دارد.
خواص اتم
- قسمت اعظم یک اتم و در نتیجه قسمت اعظم یک عنصر ، فضای خالی است.
- کلیه جرم ماده ، در هسته آن متمرکز است. سنگینی نسبی هسته اتم ، میلیونها برابر از سنگینی نسبی ماده معمولی بیشتر است. به عنوان مثال ، هرگاه تمام هستهها و الکترونهای تشکیلدهنده تمام اتمها و مولکولهای موجود در بدن انسان را یکجا جمع کنیم بدون اینکه فضای خالی بین آنها باشد، کره کوچکی بدست خواهد آمد که به زحمت با میکروسکوپ قابل روئیت است.
- سبُکترین اتمها یعنی هیدروژن معمولی ، 16 مرتبه از اکسیژن هم سبکتر است و چون یک مولکول هم از تعداد محدودی اتم تشکیل شده است، لذا وزن آن نیز مانند وزن اتم ، رقم کوچکی است و با واحدهای معمولی نمیشود بیان کرد. بنابراین واحد کربنی را برای اندازه گیری وزن اتمی و مولکولی بکار میبریم. واحد کربنی برابر یک دوازدهم جرم اتم کربن 12 در شرایط متعارفی است.
- ابعاد اتمی را با واحدهای معمولی نمیشود اندازه گیری نمود. برای این کار از واحدهای آنگستروم و نانومتر استفاده مینمایند.
- بار الکتریکی موجود در یک الکترون از لحاظ قدرمطلق ، درست برابر است با بار موجود در یک پروتون و چون تعداد الکترونها و پرتونهای تشکیلدهنده هر اتم باهم برابر است، بنابراین اتم از لحاظ الکتریکی خنثی است.
- پروتون هسته مرکزی 12-10 مرتبه حجمش از حجم اتم کوچکتر است و تقریباً تمام وزن اتم را داراست. چون از وزن الکترون صرفنظر میشود. بنابراین این وزن اتم فوقالعاده سنگین است. به عبارتی اگر حجمی به اندازه فوت مکعب را فقط از هسته مرکزی پر کنیم، وزن مکعب مزبور برابر سه بیلیون تن (3X1015 Kg) خواهد شد .
مباحث مرتبط با عنوان
- اتم
- اتم اولیه
- الکترون
- پروتون
- پیوند شیمیایی و انواع آن
- حرکت انتقالی الکترون
- حرکت وضعی الکترون
- جرم اتمی
- جرم مولکولی
- ساختمان اتم
- عدد اکسایش
- عنصر شیمیایی
- ماده
- مدل اتمی رادرفورد
- مدل اتمی بوهر
- مولکول
- نظریه اتمی
- نوترون
- واکنش شیمیایی
- واحد کربنی
- هسته
برای نمایش آواتار خود در این وبلاگ در سایت Gravatar.com ثبت نام کنید. (راهنما)




















































ایمیل شما بعد از ثبت نمایش داده نخواهد شد